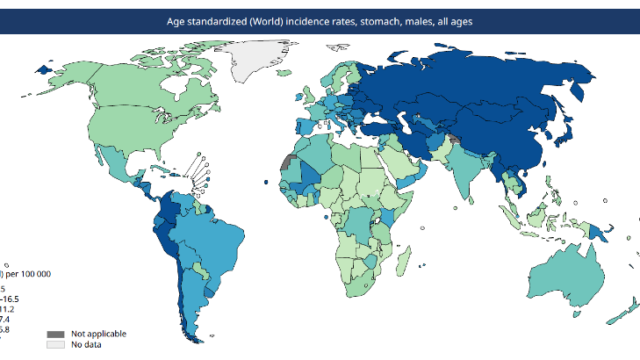
医療において薬剤疫学の役割は非常に高まっています。
例えば、医薬品を承認する前に、安全性プロファイルを理解する必要性が高まっています。
承認された医薬品でも、市販後の安全性を調査する必要性が高まっています。
また、治療効果は患者背景によって異なる場合もあるため、治療の標的とすべき集団を同定する研究を行う場合があります。
さらに、これまでの適応とは異なる、潜在的な有益性の効果を特定する場合もあります。
承認前の医薬品の安全性プロファイル
市販前試験には様々な限界と制約
理想的には、医薬品の承認前(フェーズI〜III)に安全性情報を入手することが望ましいのですが、市販前試験には限界がある。
例えば、サンプルサイズの問題です。研究規模がまれな事象 (例えば、ある事象のバックグラウンド率は5,000人に1人であった場合、2,000人の患者を対象とした研究では一般的に検出できません。
研究規模が小さい場合、頻度の低い事象 (例:治療群に3例 vs.プラセボ群に5例)について因果関係を推論するのは難しいでしょう。
さらに、RCTでは厳格な基準で参加者を選んでおり、一般的には合併症の少ない患者が選ばれることがほとんどです。
さらに、研究はアウトカムを観察するのに十分な期間ではない場合があります。
このように、市販前試験には様々な限界と制約があります。
疾患についての深い理解は必要
医薬品の安全性プロファイルを理解するには、疾患についての深い理解も必要です。これには、
- 疾患患者の臨床的な特徴
- 疾患の自然経過
- 疾患を有する患者における一般的/まれな臨床転帰
- 同じ病態の治療で使用される、別の類似した治療法に伴うリスクの理解
- 研究および治療に適した集団を特定
などが必要となります。
市販後調査研究
承認された医薬品の安全性を理解することは、以下の点からも極めて重要です:
- 安全シグナルの特定
- 治療パターンの特徴
- 治療のまれな副作用の同定/薬物-薬物相互作用の評価
安全シグナルの特定
安全信号の特定には、第IV相試験または観察研究を実施する必要があります。
治療パターンの特徴
また、治療パターンを認識する必要があり、これには:
- 誰が治療を受けているか?
- 慣習に地域差はあるか?
- 重症の患者は新しい治療法を導入されているか?
などの因子を把握する必要があります。
治療のまれな副作用の同定/薬物-薬物相互作用の評価
さらに、稀な副作用に因果関係があるのか同定する必要があります。
潜在的な薬物-薬物相互作用の評価も必要です。これは、一般的に、RCTはより健康な患者を登録するため、他の薬物との相互作用が研究されていない可能性が高いからです。
治療のターゲットとすべき集団の特定
市販後調査の目的の1つに、実質的な有効性が認められる患者集団を検索することがあります。これは、すべての患者が所定の治療に反応するわけではないからです、つまり、同じ疾患に同じ治療を行なったとしても、ごくわずかな反応しか示さない人もあれば、全く反応しない人もいます。
治療の反応性が高い人にとっては、新薬を使用することは大きな利点があります。さらに、薬剤が有効でない患者にとっては、治療により有害事象のリスクが増大するため、異なるアプローチをする必要があります。
このように治療の反応性を調査することは、疾患の生物学的な経路に関して、貴重な情報を提供する可能性があります。
有効性が認められる患者集団を特定する方法
治療の有効性が認められる一部の集団を同定する方法に、遺伝疫学的なアプローチがあります。つまり、遺伝子型が違うと薬の効果が変わるのかを調査することになります。
例えば、wild-typeのKRAS遺伝子は、転移性大腸癌患者におけるパニツムマブの有効性に重要な役割を果たしていた研究1があります:
- Wild-type: HR 0.45 [0.39, 0.59]
- Mutant: HR 0.99 [0.73, 1.36]
適用外使用の可能性
承認された薬剤には「適用症(使用しても良い疾患)」が定められています。しかし、時に適応症以外にも治療効果を認める場合があります。
例えば、スタチン(HMG-CoA還元酵素阻害薬)はコレステロール値の改善を目的に使用されています。この場合、適用症は「脂質異常症」になります。
適用外使用の例として、スタチンの糖尿病の予防効果などが挙げられます。この場合、「スタチンは糖尿病発症のリスクを低下させるか?」といった臨床的な疑問があります。
こちらに関しては、すでに市販後調査が行われており、「スタチンは糖尿病(メタアナリシスの結果)の発症リスクを低下させないと思われる」と報告2,3されています。
このように適用症以外への使用も、市販後調査を利用して臨床的な疑問を解決する必要があります。
薬剤疫学のその他の役割
薬剤疫学の市販後調査以外の役割として、
- ランダム化比較試験の設計と実施(対象集団の特定など)
- 有効性の比較研究(CER):どちらの薬が有効性・安全で優れているか?
- 費用対効果研究:私たちは利益を得るために、どのくらい費用を使うつもりか?
といった点が挙げられます。
おわりに
今回は、薬剤疫学の役割について、説明しました。
次回は、薬剤疫学でよく使用されているデータベースについて解説していきます。
参考文献
- Amado RG, Wolf M, Peeters M, et al. Wild-type KRAS is required for panitumumab efficacy in patients with metastatic colorectal cancer. J Clin Oncol. 2008;26(10):1626-1634. doi:10.1200/JCO.2007.14.7116
- Sattar N, Preiss D, Murray HM, et al. Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. Lancet (London, England). 2010;375(9716):735-742. doi:10.1016/S0140-6736(09)61965-6
- Rajpathak SN, Kumbhani DJ, Crandall J, Barzilai N, Alderman M, Ridker PM. Statin therapy and risk of developing type 2 diabetes: a meta-analysis. Diabetes Care. 2009;32(10):1924-1929. doi:10.2337/dc09-0738